- Монохлоруксусная кислота
-
Монохлоруксусная кислота 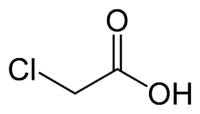
Общие Химическая формула C2H3ClO2 Физические свойства Молярная масса 94,50 г/моль Плотность 1.58 г/см³ Термические свойства Температура плавления 63 °C Температура кипения 189 °C Химические свойства pKa 2,87 Классификация Рег. номер CAS 79-11-8 RTECS AF8575000 Монохлоруксусная кислота CH2ClCOOH — бесцветные кристаллы.
Содержание
Физические свойства
tпл 61,2 °C tкип 189,3 °C. Растворима в воде, спирте, ацетоне, эфире.
Применение
Монохлоруксусная кислота — промежуточный продукт в синтезе индиго и многих др. кубовых красителей; её применяют также при получении карбоксиметилцеллюлозы, снотворного средства барбитала, гербицидов (например, солей и эфиров 2,4-дихлорфеноксиуксусной кислоты), витамина B6.
Иллюстрацией её полезности в органической химии является O-алкилирование салицилового альдегида хлоруксусной кислотой с последующим декарбоксилированием образовавшегося эфира, получая бензофуран. [1]
Большинство реакций используют высокую реакционную способность связи C-Cl. Она прекурсор для гербицида глифосата. Гербицид МХФУК(2-метил-4-хлорофенокси уксусная кислота) был получен алкилированием хлоруксусной кислотой. Хлоруксусную кислоту переводят в хлорацетилхлорид, прекурсор адреналина.
Замещение хлора серой даёт тиогликолевую кислоту, которая используется как стабилизатор ПВХ и компоненты в некоторой косметики. Наибольшее количество хлоруксусной кислоты используется для приготовления загустителя - карбоксиметилцеллюлоза.
Получение
В основном получают монохлоруксусную кислоту хлорированием ледяной уксусной кислоты при катализе уксусным ангидридом .
- CH3CO2H + Cl2 → ClCH2CO2H + HCl
Другой промышленный метод - гидролиз трихлорэтилена
- CCl2CHCl + 2 H2O → ClCH2CO2H + 2HCl
Гидролиз даёт чистый продукт, тогда как при хлорировании необходимо проводить сложную дистиляцию для отделения моно- би- трихлоруксусных кислот. [2] Годовое производство хлоруксусной кислоты составляет ориентировачно 420 тыс. тонн.
Безопасность
Как и другие галогенкислоты и галогеналканы, хлоруксусная кислота - потенциально опасный алкилирующий агент. ЛД50 на крысах 76 мг/кг
Примечания
- ↑ Burgstahler, A. W.; Worden, L. R. (1966). "Coumarone." Org. Synth. 46: 28.
- ↑ Günter Koenig, Elmar Lohmar, Norbert Rupprich "Chloroacetic Acids" in Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. DOI:10.1002/14356007.a06_537

Для улучшения этой статьи желательно?: - Найти и оформить в виде сносок ссылки на авторитетные источники, подтверждающие написанное.
Категории:- Карбоновые кислоты
- Хлорорганические соединения
- Продукция основного органического синтеза
Wikimedia Foundation. 2010.
