- Трихлорид бора
-
Трихлорид бора 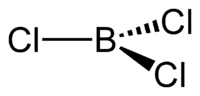
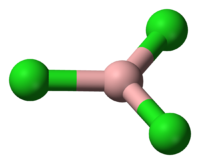

Общие Систематическое наименование хлорид бора(III) Сокращения трихлоробор Традиционные названия трихлорид бора, бора хлорид Химическая формула BCl3 Эмпирическая формула BCl3 Физические свойства Состояние (ст. усл.) бесцветный газ, дымится на воздухе Молярная масса (при 9,23 % и Cl 90,77 % по массе) 117.17 г/моль Плотность (при 0 °C) 1.326 г/см³ Термические свойства Температура плавления -107.3 °C Температура кипения 12.6 °C Температура вспышки -17 °C Критическая точка температура: 178,8 °C
давление: 3,87 мПа
плотность: 0,7 г/см³
Молярная теплоёмкость (ст. усл.) 107 Дж/(моль·К) Энтальпия образования (ст. усл.) -427 кДж/моль Давление пара (при −92 °C) 1 мм.рт.ст.
(при −68 °C) 10 мм.рт.ст.
(при −33,5 °C) 100 мм.рт.ст.
(при 20 °C) 150 кПа
Химические свойства Растворимость в воде разлагается Растворимость в остальных веществах разлагается в этаноле, растворим в тетрахлориде углерода Оптические свойства Показатель преломления 1.00139 Структура Координационная геометрия тригональная, плоская Дипольный момент 0 Д Классификация Рег. номер CAS 10294-34-5 SMILES [BH6+3].[Cl-].[Cl-].[Cl-] Регистрационный номер EC 233-658-4 RTECS ED1925000 Безопасность Токсичность Трихлорид бора — это бинарное неорганическое соединение бора и хлора с формулой BCl3. Это бесцветный газ.
Содержание
Физические свойства
При стандартных условиях трихлорид бора представляет собой тяжёлый бесцветный газ, вследствие взаимодействия с парами воды дымящийся во влажном воздухe.
При нормальных условиях — это жидкость, давление пара которой описывается уравнением:
В Твёрдом состоянии трихлорид бора образует кристаллы гексагональной сингонии, пространственная группа P63, a =0,6140 нм, c = 0,6603 нм, Z = 9.
Молекула трихлорида бора представляет собой правильный треугольник (как и другие тригалогениды бора) с длиной связи B—Cl 0,175 нм. Вследствие тригональной симметрии молекула имеет нулевой дипольный момент.
Относительное уменьшение расстояние между хлором и бором объясняется значительным вкладом π-связи.
Трихлорид бора не образует димеры, хотя есть косвенные свидетельства того, что он может образовывать димеры при очень низких температурах (20 К).
Получение
Трихлорид бора можно синтезировать из элементов:
В промышленности вместо чистого бора используют его сплавы, например ферробор.
Также в промышленности также используют метод хлорирования при температуре ~1000 °C смеси оксида бора и кокса:
В России используется промышленный метод хлорирования карбида бора при температуре 900 - 1000 °C:
Трихлорид алюминия и трифторид бора могут обмениваться галогенами:
В лабораторной практике трихлорид бора получают разложением его аддуктов, например, BCl3S(СН3)2, которые удобны в работе, т.к. являются твёрдыми веществами:
Химические свойства
Полностью гидролизуется водой с выделением большого количества тепла:
Реагирует с разбавленными и концентрированными щелочами:
Восстанавливается водородом до бора или борана:
Горит в кислороде (на воздухе при температуре >400°С):
Фтор вытесняет хлор из соединения:
Трихлорид бора является кислотой Льюиса, которая образует аддукты с третичными аминами, фосфинами, эфирами, тиоэфирами и галогенид-ионами:
Реагирует с оловоорганическими соединениями:
При пропускании через трихлорид бора электрической искры получаются низшие хлориды бора B2Cl6, B4Cl4, B8Cl8:
Реагирует со спиртами с образованием эфиров-боратов:
При нагревании реагирует с борным ангидридом с образованием оксихлорида бора:
Металлы могут восстанавливать трихлорид бора до бора или образовывать бориды:
Применение
- Треххлористый бор является исходным материалом для производства чистого бора.
- Он также используется в переработке алюминия, магния, цинка и сплавов меди для удаления нитридов, карбидов и оксидов из расплавленного металла.
- Трихлорид бора использовался как флюс для пайки сплавов алюминия, железа, цинка, вольфрама и медно-никелевого сплава.
- Обработка жидкого алюминия парами трихлорида бора улучшает качество отливок.
- Используется при изготовлении электрических сопротивлений для приклеивания углеродной пленки к керамической основе.
- Используется в плазменном травлении в производстве полупроводников.
- Используется как реагент в органическом синтезе.
Безопасность
Трихлорид бора является агрессивным реагентом.
См. также
- Список высокотоксичных газов
- Карточка вещества (англ.)
Соединения бораАрсенид бора (BAs) • Боразол (B3N3H6) • Борная кислота (H3BO3) • Борогидрид натрия (NaBH4) • Диборан (B2H6) • Карбид бора (B4C) • Метаборат натрия (NaBO2) • Нитрид бора (BN) • Оксид бора (B2O3) • Пентаборат натрия (NaB5O8) • Субоксид бора (B6O) • Сульфид бора (B2S3) • Тетраборан (B4H10) • Тетраборат натрия (Na2B4O7) • Тетрагидридоборат лития (Li[BH4]) • Тетрафторид бора (B2F4) • Тетрафтороборат водорода (H[BF4]) • Тетрафтороборат натрия (Na[BF4]) • Трибромид бора (BBr3) • Трииодид бора (BI3) • Трифторид бора (BF3) • Трихлорид бора (BCl3) • Фосфид бора (BP)
Категории:- Соединения бора
- Хлорид
- Бинарные соединения
- Высокоопасные вещества
Wikimedia Foundation. 2010.











![~\mathsf{BCl_3 + 4NaOH \rightarrow Na[B(OH)_4] + 3NaCl}](930ce023dd7205d7b0aa170be1e48290.png)










