- Ортофосфат
-
Ортофосфорная кислота 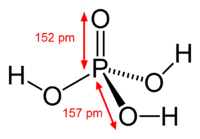
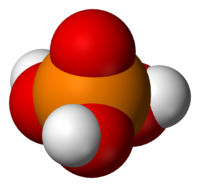
Общие Систематическое наименование Ортофосфорная кислота Химическая формула H3PO4 Отн. молек. масса 98.0 а. е. м. Молярная масса 98.0 г/моль г/моль Физические свойства Плотность вещества 1.685 (жидк) г/см³ Состояние (ст. усл.) твердое Динамическая вязкость (ст. усл.) 2.4-9.4 cПуаз Па·с
(при 20 °C)Термические свойства Температура плавления 42.35 °C Температура кипения 158 °C Химические свойства pKa 2.12, 7.21, 12.67 Растворимость в воде 548 г/100 мл Классификация номер CAS [7664-38-2]
Ортофо́сфорная кислота́ (H3PO4) — твёрдое вещество при комнатной температуре, бесцветные гигроскопичные кристаллы.При температуре выше 213 °C превращается в пирофосфорную кислоту H4P2O7. Очень хорошо растворима в воде. Обычно ортофосфорной (или просто фосфорной) кислотой называют её 85 % водный раствор (бесцветная сиропообразная жидкость без запаха). Растворима также в этаноле и других обычных растворителях.
Содержание
Получение
Фосфорную кислоту получают из фосфорита:
- Са3(PO4)2 + 3H2SO4 = 3CaSO4 + 2H3PO4
Можно получить гидролизом пентахлорида фосфора:
- PCl5 + 4 H2O → H3PO4 + 5 HCl
Или взаимодействием с водой оксида Р2O5, полученного сжиганием фосфора:
- Р2O5 + 3H2O = 2H3PO4
С водой реакция идет очень бурно, поэтому Р2O5 обрабатывают нагретым до 200° С концентрированным раствором H3PO4.
Расплавленная H3PO4 и ее концентрированные растворы обладают большой вязкостью, что обусловлено образованием межмолекулярных водородных связей.
Свойства
H3PO4 — трехосновная кислота средней силы. При взаимодействии с очень сильной кислотой, например НClO4, фосфорная кислота проявляет признаки амфотерности — образуются соли фосфорила, например [Р(ОН)4]·(ClO4).
Отличительной реакцией ортофосфорной кислоты от других фосфорных кислот явялется реакция с нитратом серебра — образуется жёлтый осадок:
- Н3РО4 + 3AgNO3 = Ag3PO4 + 3HNO3
Качественной реакцией на ион РО43- является образование ярко-жёлтого осадка молибденофосфата аммония:
- H3PO4 + 12(NH4)2MoO4 + 2HNО3 = (NH4)3PMo12O40·6H2O + 21NH4NO3 + 6Н2О
Фосфаты
Соли фосфорной кислоты называются фосфатами. Фосфорная кислота образует одно-, двух- и трехзамещенные соли.
- Н3РО4 + NaOH = NaH2PO4 + H2O (дигидрофосфат натрия)
- H3PO4 + 2NaOH = Na2HPO4 + 2H2O (гидрофосфат натрия)
- H3PO4 + 3NaOH = Na3PO4 + 3H2O (фосфат натрия)
Дигидрофосфаты (однозамещенные фосфаты) имеют кислую реакцию, гидрофосфаты (двузамещенные фосфаты) — слабощелочную, средние (трехзамещенные фосфаты, или просто фосфаты) — щелочную.
Дигидрофосфаты обычно хорошо растворимы в воде, почти все гидрофосфаты и фосфаты растворимы мало. Прокаливание солей приводит к следующим превращениям:
- NaH2PO4 = NaPO3 + H2O
- 2Na2HPO4 = Na4P2O7 + H2O
Фосфаты при прокаливании не разлагаются, исключение составляет (NH4)3PO4.
Органические фосфаты играют очень важную роль в биологических процессах. Фосфаты сахаров участвуют в фотосинтезе. Нуклеиновые кислоты также содержат остаток фосфорной кислоты.
Применение
Используется при пайке в качестве флюса (по окисленой меди, по чёрному металлу, по нержавеющей стали), для исследований в области молекулярной биологии. Применяется также для очищения от ржавчины металлических поверхностей. Образует на обработанной поверхности защитную плёнку, предотвращая дальнейшую коррозию.
Пищевая промышленность
Ортофосфорная кислота зарегистрирована в качестве пищевой добавки E338. Применяется как регулятор кислотности в газированных напитках.
Применение ортофосфорной кислоты в сельском хозяйстве. в звероводстве (в частности, при выращивании норок) используют выпойку р-ра ортофосфорной кислоты для профилактики повышенного рН желудка и мочекаменной болезни.
См. также
Источники
- Карапетьянц М. Х. Дракин С. И. Общая и неорганическая химия. М.: Химия1994
Ссылки
- Фосфорная кислота: Общие сведения о фосфорной кислоте. История открытия и получения фосфорной кислоты. Физические и химические свойства.
- Ортофосфорная кислота: Значение и применение Фосфорной кислоты.
Wikimedia Foundation. 2010.
